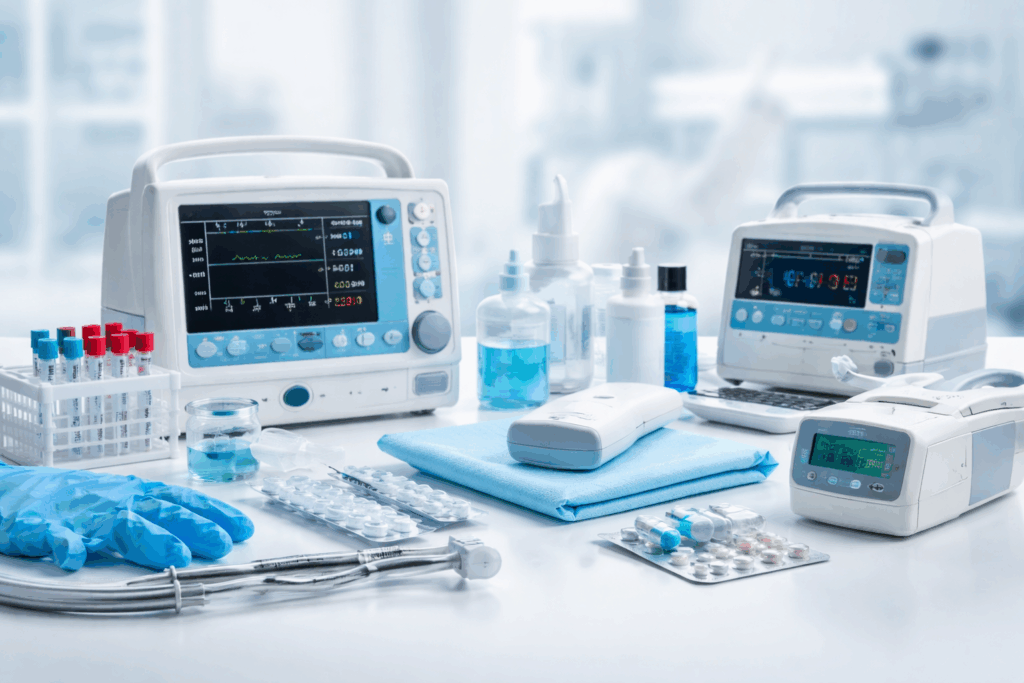
La sigla DM IIA identifica un Dispositivo Medico di Classe IIa secondo la classificazione prevista dalla normativa europea sui dispositivi medici. Si tratta di una categoria intermedia di dispositivi che presentano un livello di rischio medio-basso per il paziente e per l’utilizzatore professionale. La classificazione in Classe IIa deriva dall’applicazione delle regole contenute nel Regolamento (UE) 2017/745 (MDR), che ha sostituito la precedente Direttiva 93/42/CEE.
Dal punto di vista tecnico, un dispositivo medico di Classe IIa è destinato a essere utilizzato per finalità diagnostiche, terapeutiche o di monitoraggio e può entrare in contatto con il corpo umano in modo temporaneo o a breve termine. Rientrano in questa categoria, ad esempio, determinati dispositivi per medicazione avanzata, strumenti per aspirazione, apparecchiature diagnostiche non invasive e alcuni dispositivi riutilizzabili. La classificazione non dipende dal valore economico del prodotto, ma da criteri quali durata di utilizzo, grado di invasività, destinazione d’uso e parte del corpo coinvolta.
Rispetto ai dispositivi di Classe I (rischio basso), i DM IIa richiedono un coinvolgimento obbligatorio di un Organismo Notificato per la valutazione di conformità. Questo comporta controlli documentali, verifica del sistema qualità del fabbricante e validazione della documentazione tecnica. Rispetto alle Classi IIb e III, invece, il livello di controllo e i requisiti clinici risultano meno stringenti, pur mantenendo standard elevati di sicurezza e prestazione.
In ambito professionale – ospedaliero, ambulatoriale, RSA e strutture sanitarie – la corretta identificazione di un dispositivo medico Classe IIa è fondamentale per garantire conformità normativa, tracciabilità, appropriatezza d’uso e gestione corretta della documentazione (UDI, dichiarazione di conformità, marcatura CE).
Caratteristiche distintive del/della DM IIA
- Rischio medio-basso: livello di rischio superiore alla Classe I ma inferiore alle Classi IIb e III.
- Marcatura CE con Organismo Notificato: il numero identificativo dell’ente certificatore accompagna il marchio CE.
- Valutazione clinica obbligatoria: deve essere dimostrata sicurezza e prestazione attraverso documentazione tecnica strutturata.
- Controllo del sistema qualità: il fabbricante deve adottare un sistema conforme ai requisiti del MDR.
- Destinazione d’uso specifica: la classificazione dipende dalla funzione dichiarata e dalle modalità di utilizzo.
Dove viene utilizzato il DM IIA
I dispositivi medici di Classe IIa sono utilizzati principalmente in contesti sanitari strutturati, dove è richiesto un equilibrio tra sicurezza clinica e operatività quotidiana. Possono essere impiegati in reparti ospedalieri, ambulatori specialistici, strutture socio-sanitarie, studi odontoiatrici e centri diagnostici.
Applicazioni professionali
Settore medicale
Impiego in ospedali, cliniche private, RSA e poliambulatori per attività diagnostiche, terapeutiche e di supporto clinico. La classificazione IIa garantisce un adeguato livello di controllo normativo.
Hotel con servizio sanitario interno
Strutture alberghiere con presidio medico o infermieristico possono utilizzare dispositivi IIa per gestione di medicazioni o monitoraggi di base.
Industria sanitaria e distribuzione B2B
Grossisti e fornitori professionali devono verificare corretta marcatura CE, documentazione tecnica e tracciabilità per la commercializzazione.
Vantaggi e limiti del/della DM IIA
Vantaggi
- Elevato standard di sicurezza: la valutazione da parte di un Organismo Notificato aumenta l’affidabilità del dispositivo.
- Conformità regolatoria chiara: inquadramento preciso secondo MDR 2017/745.
- Adatto a contesti clinici strutturati: equilibrio tra rischio controllato e ampiezza di utilizzo.
Limiti e aspetti da considerare
- Iter certificativo più complesso rispetto alla Classe I: maggiori costi e tempi per il fabbricante.
- Obblighi documentali stringenti: necessaria gestione accurata di fascicolo tecnico e sorveglianza post-commercializzazione.
- Non idoneo per applicazioni ad alto rischio: per utilizzi critici è richiesta Classe IIb o III.
Domande frequenti su DM IIA
Cosa significa dispositivo medico di classe IIa?
Un dispositivo medico di Classe IIa è un prodotto destinato a finalità diagnostiche o terapeutiche che presenta un livello di rischio medio-basso. La classificazione viene stabilita in base a criteri come durata di utilizzo, invasività e destinazione d’uso. Rispetto alla Classe I, richiede la valutazione di conformità da parte di un Organismo Notificato e una documentazione tecnica più strutturata. È regolamentato dal Regolamento (UE) 2017/745 (MDR) e deve riportare marcatura CE con numero identificativo dell’ente certificatore.
Quali sono le classi di dispositivi medici?
I dispositivi medici sono suddivisi in quattro classi di rischio: Classe I (rischio basso), Classe IIa (rischio medio-basso), Classe IIb (rischio medio-alto) e Classe III (rischio elevato). La classificazione dipende da fattori quali invasività, durata di contatto con il corpo umano e funzione clinica. All’aumentare della classe cresce il livello di controllo normativo, la complessità della valutazione clinica e il coinvolgimento dell’Organismo Notificato.
Qual è la normativa di riferimento?
La normativa di riferimento per i dispositivi medici di Classe IIa è il Regolamento (UE) 2017/745 (MDR), pienamente applicabile dal 26 maggio 2021. Il regolamento stabilisce criteri di classificazione, requisiti di sicurezza e prestazione, obblighi di sorveglianza post-commercializzazione e sistema UDI per la tracciabilità. In Italia, il MDR è integrato dalle disposizioni nazionali di adeguamento e dai controlli del Ministero della Salute.
Conclusione
La sigla DM IIA identifica una categoria strategica di dispositivi medici ampiamente utilizzata in ambito sanitario professionale. Comprendere il significato della Classe IIa è essenziale per operatori, responsabili acquisti e distributori B2B, poiché incide su obblighi documentali, tracciabilità e conformità normativa. Una corretta classificazione garantisce sicurezza clinica, rispetto del MDR e adeguata gestione del rischio lungo tutta la filiera.