Cos’è un DM di Classe I
Il termine DM Classe I identifica un dispositivo medico di classe I, ovvero un prodotto sanitario che, secondo la classificazione europea, presenta un basso livello di rischio per il paziente e per l’utilizzatore. La classificazione dei dispositivi medici è regolata dal Regolamento (UE) 2017/745 (MDR), che ha sostituito la precedente Direttiva 93/42/CEE, introducendo criteri più rigorosi in termini di sicurezza, tracciabilità e sorveglianza post-commercializzazione.
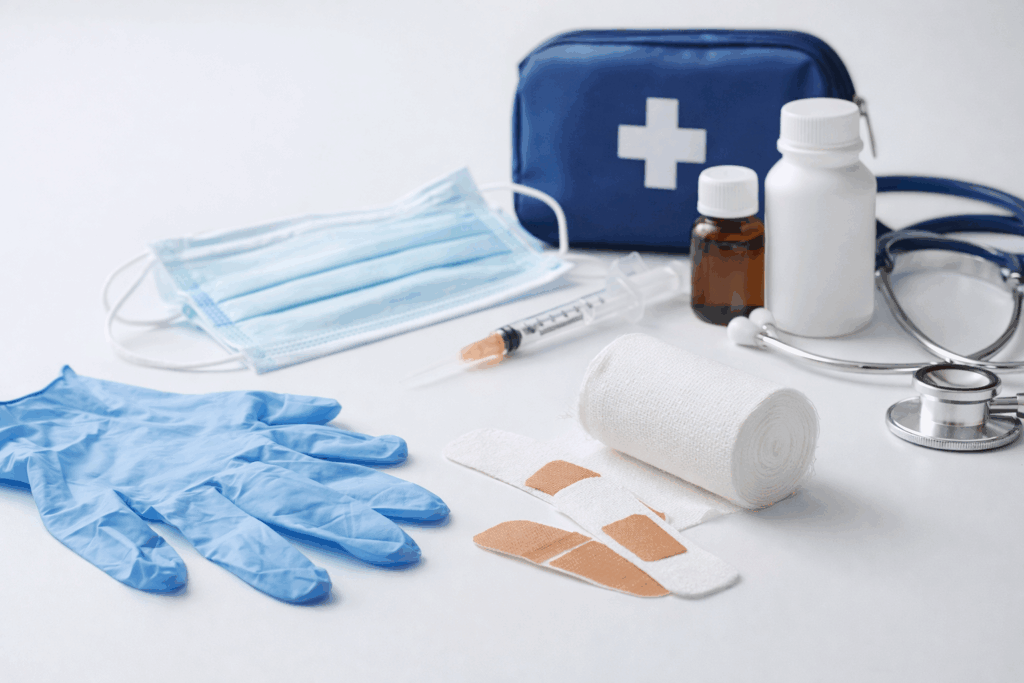
Un dispositivo medico è definito come qualsiasi strumento, apparecchio, materiale o altro articolo destinato dal fabbricante a essere impiegato sull’uomo per finalità diagnostiche, preventive, terapeutiche o di monitoraggio. I dispositivi medici di classe I comprendono generalmente prodotti non invasivi, senza funzione attiva o con impatto clinico limitato. Esempi tipici includono guanti da visita non sterili, camici monouso, mascherine chirurgiche (quando classificate come DM), bende, cerotti e altri articoli di uso sanitario comune.
Dal punto di vista normativo, i DM di Classe I possono essere immessi sul mercato tramite autocertificazione del fabbricante, che redige la dichiarazione di conformità e appone la marcatura CE, salvo i casi particolari di dispositivi sterili o con funzione di misura, che richiedono l’intervento di un organismo notificato. Rispetto alle classi superiori (IIa, IIb e III), i requisiti documentali e di valutazione clinica risultano meno complessi, ma rimangono obbligatori sistemi di gestione della qualità, analisi dei rischi e tracciabilità.
Nel contesto professionale B2B – ambito medicale, RSA, studi dentistici, ambulatori, ma anche strutture alberghiere e servizi di assistenza – la corretta identificazione di un DM Classe I è fondamentale per garantire conformità normativa, corretta fatturazione IVA e adeguata gestione documentale. La distinzione rispetto ai DPI (Dispositivi di Protezione Individuale) è particolarmente rilevante: mentre i DPI tutelano l’operatore, il dispositivo medico è destinato primariamente alla protezione o al trattamento del paziente.
Caratteristiche distintive del DM Classe I
- Basso livello di rischio: prodotti considerati a rischio minimo per pazienti e operatori, secondo le regole di classificazione MDR.
- Marcatura CE obbligatoria: attestazione di conformità ai requisiti essenziali di sicurezza e prestazione previsti dal Regolamento europeo.
- Autocertificazione del fabbricante: nella maggior parte dei casi non è richiesto l’intervento di un organismo notificato.
- Documentazione tecnica: fascicolo tecnico, valutazione dei rischi e sorveglianza post-market sono comunque obbligatori.
- Tracciabilità: identificazione del prodotto, lotto e fabbricante per garantire controllo lungo la filiera.
Dove viene utilizzato il DM Classe I
I dispositivi medici di Classe I trovano impiego in numerosi contesti professionali dove è richiesta una protezione sanitaria di base o un supporto alle attività cliniche non invasive.
Applicazioni professionali
- Settore medicale: ambulatori, studi dentistici, cliniche e RSA utilizzano DM Classe I per medicazioni, visite, protezione del paziente e gestione dell’igiene.
- Hotel e strutture ricettive: impiego in kit di primo soccorso e nella gestione di emergenze sanitarie di base.
- Pulizia professionale: utilizzo in contesti sanitari e socio-assistenziali per garantire standard igienici conformi alle normative vigenti.
- Industria: presenza in infermerie aziendali e postazioni di primo intervento sanitario.
Vantaggi e limiti del DM Classe I
Vantaggi
- Semplicità normativa: iter di immissione sul mercato meno complesso rispetto alle classi superiori.
- Costi contenuti: generalmente più accessibili rispetto a dispositivi a rischio medio o alto.
- Ampia diffusione: prodotti facilmente reperibili e adatti a molteplici contesti professionali.
- Conformità europea: garantiscono rispetto degli standard di sicurezza previsti dal MDR.
Limiti e aspetti da considerare
- Ambito di utilizzo limitato: non idonei per procedure invasive o ad alto rischio clinico.
- Distinzione da DPI: è necessario verificare correttamente la classificazione per evitare errori normativi o fiscali.
- Responsabilità del fabbricante: l’autocertificazione comporta obblighi stringenti in termini di documentazione e controllo qualità.
Domande frequenti su DM Classe I
Quali sono i dispositivi medici classe 1?
I dispositivi medici di Classe I sono prodotti a basso rischio destinati a finalità sanitarie non invasive o con impatto clinico minimo. Rientrano in questa categoria articoli come guanti da visita non sterili, bende, cerotti, camici monouso, mascherine chirurgiche (quando classificate come DM) e strumenti semplici per medicazione. La classificazione avviene secondo le regole del Regolamento (UE) 2017/745, che valuta grado di invasività, durata del contatto e finalità d’uso. Sono generalmente soggetti ad autocertificazione con marcatura CE.
Come sono classificati i dispositivi medici?
I dispositivi medici sono classificati in Classe I, IIa, IIb e III in base al livello di rischio associato al loro utilizzo. I criteri di classificazione previsti dal Regolamento (UE) 2017/745 tengono conto di fattori come invasività, durata del contatto con il paziente, parte del corpo interessata e funzione del dispositivo. La Classe I rappresenta il livello di rischio più basso, mentre la Classe III comprende dispositivi ad alto rischio, come impianti o apparecchiature invasive critiche.
Qual è la normativa vigente?
La normativa vigente in materia di dispositivi medici è il Regolamento (UE) 2017/745 (MDR), applicabile in tutti gli Stati membri dell’Unione Europea. Il regolamento stabilisce requisiti stringenti in termini di sicurezza, valutazione clinica, tracciabilità (UDI), sorveglianza post-commercializzazione e responsabilità degli operatori economici. Ha sostituito la Direttiva 93/42/CEE, introducendo un sistema più rigoroso e uniforme per garantire elevati standard di tutela della salute pubblica.
Conclusione
Il DM Classe I rappresenta una categoria fondamentale nel panorama dei dispositivi medici, soprattutto per le strutture professionali che necessitano di prodotti sicuri, conformi e a basso rischio. Conoscere classificazione, ambito di utilizzo e riferimenti normativi consente a operatori sanitari, responsabili acquisti e aziende B2B di effettuare scelte consapevoli, garantendo conformità al Regolamento europeo e corretta gestione documentale lungo tutta la filiera.